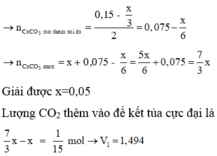Sục V lít khí CO2 qua 150g dd Ca(OH)2 2,96%.Tính V để:
a) Không thu được kết tủa.
b) Thu được kết tủa lớn nhất.
c) Được 3g kết tủa.
Bạn nào giỏi Hóa 9 thì giải bài này chi tiết hộ mình với nhé!
Bài 23. Sục V(l) CO2(đkc) vào 150ml dd Ba(OH)2 1M, sau phản ứng thu được 19,7g kết tủa. Tìm V.
Bài 24. Cho 2,24 lít khí CO2 (đkc) tác dụng vừa đủ với 200ml dd Ca(OH)2 sinh ra chất kết tủa trắng. Tính nồng độ mol/lít của dung dịch Ca(OH)2
Bài 25. Hấp thụ hoàn toàn a mol khí CO2 vào dung dịch chứa b mol Ca(OH)2 thì thu được hỗn hợp 2 muối CaCO3 và Ca(HCO3)2. Tìm mối liên hệ giữa a và b.
Bài 26. Hấp thụ hoàn toàn 2,688 lít khí CO2(đkc) vào 2,5 lít dd Ba(OH)2 nồng độ a mol/lít,thu được 15,76g kết tủa .Tìm a.
Bài 27. Hấp thụ hoàn toàn 2,24 lít CO2(đkc)vào dd nước vôi trong có chứa 0,25 mol Ca(OH)2. Xác định sản phẩm muối thu được sau phản ứng.
ai trả lời hết tôi tick cho nhiều câu trả lời khác
Bài 23 :
n BaCO3 = 0,1(mol) > n Ba(OH)2 = 0,15 mol
- TH1 : Ba(OH)2 dư
$Ba(OH)_2 + CO_2 \to BaCO_3 + H_2O$
n CO2 = n BaCO3 = 0,1(mol)
=> V = 0,1.22,4 = 2,24 lít
- TH1 : BaCO3 bị hòa tan một phần
$Ba(OH)_2 + CO_2 \to BaCO_3 + H_2O(1)$
$Ba(OH)_2 + 2CO_2 \to Ba(HCO_3)_2(2)$
n CO2(1) = n Ba(OH)2 (1) = n BaCO3 = 0,1(mol)
=> n Ba(OH)2 (2) = 0,15 - 0,1 = 0,05(mol)
=> n CO2 (2) = 2n Ba(OH)2 (2) = 0,1(mol)
=> V = (0,1 + 0,1).22,4 = 4,48 lít
Bài 24 :
$Ca(OH)_2 + CO_2 \to CaCO_3 + H_2O$
n Ca(OH)2 = n CO2 = 2,24/22,4 = 0,1(mol)
CM Ca(OH)2 = 0,1/0,2 = 0,5M
Bài 27 :
n CO2 = 0,1(mol)
Ta có :
n CO2 / n Ca(OH)2 = 0,1/0,25 = 0,4 < 1
Do đó, sản phẩm muối gồm CaCO3 do Ca(OH)2 dư
Câu 25 :
$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
$2CO_2 + Ca(OH)_2 \to Ca(HCO_3)_2$
Vì thu được hai muối nên :
1 < a/b < 2
<=> b < a < 2b
Sục V lít khí CO2 ở đktc vào 0.2 lít dd Ca(OH)2 0.5 M thu được 2.5 g kết tủa. tính V?
Ta có : nCa(OH)2 = 0,2 . 0,5 = 0,1 (mol)
n CaCO3 = 2,5 : 100 = 0,025 mol
Khi sục V lít khí CO 2 vào dung dịch Ca(OH)2 thì có thể xảy ra 2 trường hợp sau :
Trường hợp 1: Ca(OH)2 tác dụng vừa đủ hoặc dư , còn khí CO2 tác dụng hết . Chỉ xảy ra phản ứng sau :
CO2 + Ca(OH)2 = CaCO3 + H2O ( 1 )
0,025 < ----- 0,025 <-----0,025 mol
số mol Ca(OH)2 phản ứng = 0,025 mol < 0,1 mol (phù hợp )
Vậy n CO2 là 0,025 mol => V = 0,025 . 22,4 = 0,56 lít
Trường hợp 2 : Ca(OH)2 tác dụng hết , khí CO2 có dư sau phản ứng ( 1 ) . Trước hết xảy ra phản ứng ( 1 )
CO2 + Ca(OH)2 = CaCO3 + H2O ( 1 )
0,1 mol <----0,1 mol -----> 0,1 mol
Sau khi (1) kết thúc , lượng Ca(OH)2 cũng hết , khí cacbonic còn dư sau pư sẽ tiếp tục phản ứng với muối CaCO3 tạo thành ( làm giảm bớt lượng kết tủa sau pư 1 )
CO2 + H2O + CaCO3 = Ca(HCO3)2 (2)
0,075 mol <------------ 0,1 - 0,025 = 0,075
Vậy tổng số mol khí CO 2 thổi vào là 0,1 + 0,075 = 0,175 mol
=> V = 0,175 . 22,4 = 3,92 lít
\(n_{Ca\left(OH\right)_2}=0,5.0,2=0,1\left(mol\right)\)
PTHH : CO2 + Ca(OH)2 -----> CaCO3 + H2O
=> \(n_{CaCO_3}=\frac{2,5}{100}=0,025\left(mol\right)\)
Ta có \(\frac{n_{Ca\left(OH\right)_2}\left(\text{bài ra}\right)}{n_{Ca\left(OH\right)_2}\left(\text{phương trình}\right)}=\frac{0,1}{1}>\frac{n_{CaCO_3}\left(\text{bài ra}\right)}{n_{CaCO_3}\left(\text{phương trình}\right)}=\frac{0,025}{1}\)
=> CaCO3 phản ứng hết , Ca(OH)2 dư
Suy ra nCO2 = 0,025 mol
=> VCO2 = 0,025 . 22,4 = 0,56 (lít)
trong trường hợp,ta không bận tâm pư tạo muối nào vì ta biết muối CaCO3 kết tủa nên sản phẩm không
nCa(OH)2 = 0,2 . 0,5 = 0,1 (mol)
n CaCO3 = 2,5 : 100 = 0,025 mol
Khi sục V lít khí CO 2 vào dung dịch Ca(OH)2 thì có thể xảy ra 2 trường hợp sau :
Trường hợp 1: Ca(OH)2 tác dụng vừa đủ hoặc dư , còn khí cacbonic tác dụng hết . Chỉ xảy ra phản ứng sau :
CO 2 + Ca(OH)2 = CaCO 3 + H2O ( 1 )
0,025 < ----- 0,025 <-----0,025 mol
số mol Ca(OH)2 phản ứng = 0,025 mol < 0,1 mol (phù hợp )
Vậy n CO 2 là 0,025 mol => V = 0,025 . 22,4 = 0,56 lít
Trường hợp 2 : Ca(OH)2 tác dụng hết , khí CO 2 có dư sau phản ứng ( 1 ) . Trước hết xảy ra phản ứng ( 1 )
CO 2 + Ca(OH)2 = CaCO 3 + H2O ( 1 )
0,1 mol <----0,1 mol -----> 0,1 mol
Sau khi (1) kết thúc , lượng Ca(OH)2 cũng hết , khí cacbonic còn dư sau pư sẽ tiếp tục phản ứng với muối CảCO tạo thành ( làm giảm bớt lượng kết tủa sau pư 1 )
CO2 + H2O + CaCO3 = Ca(HCO3)2 (2)
0,075 mol <------------ 0,1 - 0,025 = 0,075
Vậy tổng số mol khí CO 2 thổi vào là 0,1 + 0,075 = 0,175 mol
=> V = 0,175 . 22,4 = 3,92 lít
Chúc em học tốt !!!
Sục từ từ V lít CO2 vào 800ml dung dịch A gồm KOH 0,05M và Ca(OH)2 0,02M
a)tính V để thu được lượng kết tủa lớn nhất
b)Tính V để thu được lượng kết tủa là 1 gam
c)tính kết tủa thu được khi V=13,44 lít
\(CO_2+Ca(OH)_2\to CaCO_3\downarrow+H_2O\\ CO_2+2KOH\to K_2CO_3+H_2O\\ CO_2+H_2O+K_2CO_3\to 2KHCO_3\\ CO_2+H_2O+CaCO_3\to Ca(HCO_3)_2\\ a,n_{KOH}=0,05.0,8=0,04(mol);n_{Ca(OH)_2}=0,02.0,8=0,016(mol)\\ m_{{CaCO_3}_{max}}\Rightarrow \text{chưa có p/ứ hòa tan kết tủa}\\ \Rightarrow \begin{cases} \text{chỉ xảy ra p/ứ tạo KT: }n_{CO_2}=0,016(mol)\\ \text{chỉ xảy ra p/ứ tạo }KHCO_3:n_{CO_2}=0,016+0,04=0,056(mol) \end{cases}\\ \text{Vậy }m_{{CaCO_3}_{max}}\Leftrightarrow 0,016{<}n_{CO_2}{<}0,056\)
\(b,n_{CaCO_3}=\dfrac{1}{100}=0,01(mol)\\ 0,01{<}0,016\Rightarrow \text{xảy ra 2 TH}\\ TH_1:\text{chỉ xảy ra p/ứ tạo KT }\Rightarrow n_{CO_2}=0,01(mol)\Rightarrow V_{CO_2}=0,224(l)\\ TH_2:\text{xảy ra p/ứ hòa tan }\Rightarrow n_{CaCO_3(\text{hòa tan})}=0,016-0,01=0,006(mol)\\ \Rightarrow n_{CO_2}=0,006+0,016+0,04=0,062(mol)\\ \Rightarrow V_{CO_2}=0,062.22,4=1,3888(l)\\ c,Sửa:V=1,344(l)\\ n_{CO_2}=0,06(mol)\Rightarrow n_{CaCO_3(\text{ hòa tan})}=0,06-0,04-0,016=0,004(mol)\\ \Rightarrow n_{CaCO_3}=0,016-0,004=0,012(mol)\\ \Rightarrow m_{CaCO_3}=0,012.100=1,2(g)\)
Sục từ từ v lít khí co2 vào 100ml dd ba(oh)2 1 M , sau khi phản ứng hoàn toàn thu được 15,76g kết tủa. Lọc bớt kết tủa, đun nóng nước lọc thu thêm được m gam kết tủa. Tính V và m
6/ A/ Cho hoàn toàn V lít khí CO2 (ở đktc) từ từ đi qua 200 ml dung dịch Ca(OH)2 2M. Sau khi phản ứng kết thúc thu được 20 gam chất kết tủa. Tìm giá trị của V? B/ Sục x(lit) CO2 (đktc) vào 400ml dung dịch Ba(OH)2 0,5M thì thu được 4,925g kết tủa. Tính x. C/ Dẫn 4,48 lít khí SO2 (đktc) vào một bình chứa 120g dung dịch NaOH 12,5%. Tính nồng độ % của dung dịch muối thu được? Các phản ứng xảy ra hoàn toàn.
a, Ta có : \(\left\{{}\begin{matrix}n_{CaCO3}=\dfrac{m}{M}=0,2\left(mol\right)\\n_{Ca\left(OH\right)2}=C_M.V=0,4\left(mol\right)\end{matrix}\right.\)
\(BTNT\left(Ca\right):n_{Ca\left(HCO_3\right)_2}=n_{Ca\left(OH\right)2}-n_{CaCO3}=0,2\left(mol\right)\)
\(BTNT\left(C\right):n_{CO2}=n_{CaCO3}+2n_{Ca\left(HCO3\right)2}=0,6\left(mol\right)\)
\(\Rightarrow V_{CO2}=13,44l\)
b, Ta có : \(\left\{{}\begin{matrix}n_{BaCO3}=\dfrac{m}{M}=0,025\left(mol\right)\\n_{Ba\left(OH\right)2}=C_M.V=0,2\left(mol\right)\end{matrix}\right.\)
\(BTNT\left(Ba\right):n_{Ba\left(HCO_3\right)_2}=n_{Ba\left(OH\right)2}-n_{BaCO3}=0,175\left(mol\right)\)
\(BTNT\left(C\right):n_{CO2}=n_{BaCO3}+2n_{Ba\left(HCO3\right)2}=0,375\left(mol\right)\)
\(\Rightarrow V_{CO2}=8,4l\)
c, Ta có : \(1< T=\dfrac{n_{NaOH}}{n_{SO2}}=1,875< 2\)
- Áp dụng phương pháp đường chéo :
Ta được : \(\dfrac{n_{NaHSO3}}{n_{Na2SO3}}=\dfrac{1}{7}\)
\(\Leftrightarrow7n_{NaHSO3}-n_{Na2SO3}=0\)
\(BTNT\left(Na\right):n_{NaHSO3}+2n_{Na2SO3}=0,375\)
\(\Rightarrow\left\{{}\begin{matrix}n_{NaHSO3}=0,025\\n_{Na2SO3}=0,175\end{matrix}\right.\)
\(\Rightarrow m_M=24,65g\)
giải giúp mình bài này mà khồng pt ion
Dung dịch X chứa NaOH 0,2M và Ca(OH)2 0,1M. Sục 7.84 lít khí CO2 (đktc) vào 1 lít dung dịch X thì khối lượng kết tủa thu được là?
kh dùng pt ion thì dùng pt thường cũng đc nhỉ
nNaOH = 0,2 (mol)
nCa(OH)2 = 0,1 (mol)
nCO2 = 0,35 (mol)
PTHH : CO2 + Ca(OH)2 ----> CaCO3 + H2O
0,1<--------0,1 -----------> 0,1 (mol)
CO2 + 2NaOH -----------> Na2CO3 + H2O
0,1<-----0,2---------------> 0,1 (mol)
CO2 + Na2CO3 + H2O----------> 2NaHCO3
0,1<--- 0,1 --------------------> 0,2 (mol)
CO2 + CaCO3 + H2O -------> Ca(HCO3)2
0,05 ---> 0,05 ---------------> 0,05 (mol)
=> nCaCO3 thu được = 0,1 - 0,05 = 0,05 (mol)
=> mCaCO3 = 0,05.100 = 5 (g)
Dẫn V lít khí C O 2 ở đktc vào 0,3 lít dd C a ( O H ) 2 0,02M thì thu được 0,2 gam kết tủa. Tính giá trị của V.
Sục V lít CO2 vào 300ml dd X gồm NaOH 1M và Ca(OH)2 1M, sau phản ứng thu được 98,5g kết tủa. Tính V.
Hấp thụ hoàn toàn V lít CO2 vào dung dịch Ca(OH)2 aM thì thu được m1 gam kết tủa. Cùng hấp thụ (V + 3,36) lít CO2 vào dung dịch Ca(OH)2 thì thu được m2 gam kết tủa. Nếu thêm (V + V1) lít CO2 vào dung dịch Ca(OH)2 trên thì thu được lượng kết tủa cực đại. Biết m1 bằng 3/7 khối lượng kết tủa cực đại và m1:m2 = 3:2. Các thể tích khí đều đo ở đktc. Giá trị của V1 gần nhất với
A. 2,016
B. 1,494
C. 0,672
D. 1,00
Đáp án B
Gọi x là số mol CO2 (tương đương V lít).
Lúc cho V lít CO2 thu được x mol kết tủa CaCO3.
Cho cho V+3,36 lít CO2 vào thì chỉ thu được 2/3 lượng kết tủa tức 2x/3 mol CaCO3.
Vậy lượng 0,15 mol CO2 thêm vào đã tạo thêm một lượng kết tủa và hòa tan lượng kết tủa đó và hòa tan thêm x/3 mol kết tủa nữa